ADENOCARCINOMA COLORRECTAL (TIPO USUAL)
Es una patología neoplásica invasiva de estirpe epitelial. Puede presentarse de novo o en una menor proporción, asociado a síndromes familiares (10%). La mayoría de los CRC surgen a partir de pólipos precancerosos (ya sean de tipo convencional o aserrados) que de por sí ya cuentan con mutaciones genéticas propias que favorecen su génesis. Por lo que se considera una enfermedad molecularmente heterogénea que incluye (entre otras) alteraciones en APC, KRAS, TP53, SMAD4, PIK3CA, MLH1 y MSH2. Representa más del 90% de las neoplasias malignas de colon.
- Se puede localizar a cualquier nivel del marco colónico o en recto
- Predilección por el colon izquierdo y recto
- Clasificación por localización:
- Carcinomas del colon derecho o proximal: ciego, colon ascendente y/o transverso (2/3 proximales). Usualmente son tumores con inestabilidad de microsatélites y surgen de lesiones aserradas sésiles.
- Carcinomas de colon izquierdo: desde el tercio distal del colon transverso hasta el colon sigmoides. Son tumores que muestran en su gran mayoría vía de inestabilidad cromosomal y surgen por lo general de adenomas convencionales.
- Carcinomas de recto
- Inicialmente los CRC izquierdos suelen tener un aspecto polipoide mientras que los derechos, una morfología plana.
- En estadios avanzados los CRC izquierdos y de recto se muestran como lesiones anulares y constrictivas, mientras que derechos suelen presentarse como masas exofíticas de mayor tamaño.
- Tipos macroscópicos (similar a clasificación de Borrmann para cáncer gástrico):
- Fungoide/polipoide
- Úlcero-fungoide
- Úlcero-infiltrativo
- Infiltrativo
- Número: usualmente lesiones únicas (tumores sincrónicos son infrecuentes)
- Células con atipia nuclear con mitosis atípicas
- Forman glándulas dilatadas, deformadas, irregulares de bordes angulosos o muy aglomeradas o fusionadas (estructuras cribiformes)
- Presencia de necrosis en el lumen glandular ("necrosis sucia")
- Crecimiento tipo Gemaciones o "budding" (1 célula tumoral o grupo ≤4 células), asociado a mal pronóstico
- Grupos tumorales con más de 5 células en ausencia de formación glandular se denominan "grupos pobremente diferenciados"
- Desmoplasia (proliferación fibrosa que rodea células tumorales) - criterio importante para demostrar invasión
- Linfocitos infiltrantes en el tumor (TILs) compuestos por linfocitos T citotóxicos (T CD8), T colaboradores (T CD4) y células NK
- Infiltrar la lámina propia por una célula tumoral o un grupo pequeño
- Respuesta estromal (inflamación o desmoplasia)
- Anaplasia nuclear y severa alteración de la arquitectura
- Patrón de tinción citoplasmático
- Útil para diagnóstico diferencial de metástasis de origen desconocido junto a CK7
- CRC suelen tener inmunofenotipo CK20+/CK7- (20% pueden ser CK20-/CK7+ o CK20-/CK7-)
- Expresión ausente de CK20 asociada a inestabilidad de microsatélite
- Positividad nuclear indica diferenciación intestinal
- Negatividad indica pérdida de función reparadora (inestabilidad de microsatélite)
- Patrón de tinción nuclear
- Positivo en carcinoma colorrectal (especificidad ~100% con CK20+/CK7-)
- Útil para distinguir CRC de neoplasias gástricas o pancreáticas (negativas)
- Infiltración neoplásica en la submucosa (reconocida por desmoplasia o vasos de paredes gruesas)
- Características que definen el tipo histológico correspondiente
- Tipo histológico (y grado si es NOS)
- Profundidad de la invasión
- Invasión perineural
- Invasíon vascular (intra y extramural)
- Invasíon linfática
- Gemaciones
- Estado de márgenes (en cáncer rectal margen circunferencial ≤1 mm se considera positivo)
- Estado de ganglios linfáticos (en resecciones tumorales)
- Adenocarcinoma, NOS: representa el 90% de todos los CRC (tipo "usual")
- Otros subtipos:
- Adenocarcinoma mucinoso
- Carcinoma de células en anillo de sello
- Carcinoma medular
- Adenocarcinoma aserrado
- Adenocarcinoma micropapilar
- Carcinoma adenoescamoso
- Adenocarcinoma tipo adenoma
- Carcinomas con componente sarcomatoide
- Carcinoma indiferenciado
| Grado | Descripción | % Formación glandular |
|---|---|---|
| Bien diferenciado | Glándulas bien formadas con mínima atipia | >95% |
| Moderadamente diferenciado | Glándulas evidentes con áreas sólidas | 50-95% |
| Pobremente diferenciado | Pocas glándulas reconocibles | 5-49% |
| Indiferenciado | Sin formación glandular | <5% |
Notas:
- La gradación se basa en el componente menos diferenciado (gradación definitiva en pieza quirúrgica)
- Mayor grado histológico generalmente implica peor pronóstico
- Tumor en la pared colónica
- Estado de los ganglios linfáticos
- Presencia de metástasis a distante
- Intraepitelial: No rompe membrana basal (neoplasias intraepiteliales o displasias de alto grado)
- Intramucoso: Rompe membrana basal pero no alcanza submucosa (carcinoma intramucoso)
- Submucosa: Compromiso de submucosa (pT1 - mínimo para CRC invasivo)
- Capa muscular: Compromiso de capa muscular (pT2)
- Subserosa: Compromiso de subserosa (T3)
- Serosa: Extensión sobre serosa (T4a)
*Compromiso de capa muscular y subserosa solo se estudia en pieza quirúrgica
- Recomendación: Disecar al menos 12 ganglios para considerarlo representativo
- Clasificación de metástasis:
- Células tumorales aisladas: <0.2 mm (AJCC: pN0)
- Micrometástasis: 0.2-2 mm (ganglio comprometido)
- Depósitos tumorales: Nódulos tumorales sin tejido linfoide (solo se considera invasión si hay vasos/nervios)
- Fibrosis estromal
- Moderado infiltrado inflamatorio mononuclear
- Macrófagos espumosos y hemosiderófagos
- Lagos de mucina ("mucina acelular" = respuesta patológica completa)
- Otros cambios estromales: edema, cambios mixoides, necrosis, calcificaciones
- Reducción de población neoplásica
- Cambios citológicos: eosinofilia citoplasmática hasta aspecto escamoso
| Sistema | Grado | Descripción |
|---|---|---|
| Dworak/Mandard | 0 | Sin regresión |
| 1 | Regresión mínima (fibrosis con tumor residual) | |
| 2 | Regresión moderada (fibrosis y vasos con tumor residual) | |
| 3 | Buena regresión (muy pocas células tumorales) | |
| 4 | Regresión completa (sin células tumorales) | |
| AJCC | 1 | Sin respuesta (tumor residual >50%) |
| 2 | Respuesta parcial (tumor residual 1-50%) | |
| 3 | Respuesta completa (tumor residual 0%) |
- Nagtegaal ID, Arends MJ, Salto-Tellez M. Colorectal adenocarcinoma. In WHO classification of Tumors Digestive system tumours. Lyon (France): International Agency for Research on Cancer, 2019. p 177-187.
- Fleming M, Ravula S, Tatishchev SF, Wang HL. Colorectal carcinoma: Pathologic aspects. J Gastrointest Oncol. 2012;3(3):153-173. doi:10.3978/j.issn.2078-6891.2012.030
- Kim BH, Kim JM, Kang GH, Chang HJ, Kang DW, Kim JH, Bae JM, Seo AN, Park HS, Kang YK, Lee KH, Cho MY, Do IG, Lee HS, Chang HK, Park DY, Kang HJ, Sohn JH, Chang MS, Jung ES, Jin SY, Yu E, Han HS, Kim YW. Standardized Pathology Report for Colorectal Cancer, 2nd Edition. J Pathol Transl Med. 2020 Jan;54(1):1-19. doi: 10.4132/jptm.2019.09.28. Epub 2019 Nov 13. PMID: 31722452; PMCID: PMC6986966.
- Noack, P., Langer, R. Molecular pathology of colorectal cancer. memo 16, 116-121 (2023). https://doi.org/10.1007/s12254-023-00893-2
- Baran B, Mert Ozupek N, Yerli Tetik N, Acar E, Bekcioglu O, Baskin Y. Difference Between Left-Sided and Right-Sided Colorectal Cancer: A Focused Review of Literature. Gastroenterology Res. 2018 Aug;11(4):264-273. doi: 10.14740/gr1062w. Epub 2018 Feb 8. PMID: 30116425; PMCID: PMC6089587.
- Kim SH, Chang HJ, Kim DY, Park JW, Baek JY, Kim SY, Park SC, Oh JH, Yu A, Nam BH. What Is the Ideal Tumor Regression Grading System in Rectal Cancer Patients after Preoperative Chemoradiotherapy? Cancer Res Treat. 2016 Jul;48(3):998-1009. doi: 10.4143/crt.2015.254. Epub 2015 Oct 22. PMID: 26511803; PMCID: PMC4946373.
- Mik M, Berut M, Dziki L, Trzcinski R, Dziki A. Right- and left-sided colon cancer - clinical and pathological differences of the disease entity in one organ. Arch Med Sci. 2017 Feb 1;13(1):157-162. doi: 10.5114/aoms.2016.58596. Epub 2016 Mar 16. PMID: 28144267; PMCID: PMC5206358.
- Tong GJ, Zhang GY, Liu J, Zheng ZZ, Chen Y, Niu PP, Xu XT. Comparison of the eighth version of the American Joint Committee on Cancer manual to the seventh version for colorectal cancer: A retrospective review of our data. World J Clin Oncol. 2018 Nov 10;9(7):148-161. doi: 10.5306/wjco.v9.i7.148. PMID: 30425940; PMCID: PMC6230917.
- De la Cruz-Merino L, Henao F, Garcia T. Linfocitos infiltrantes de tumor: su implicación en el cáncer colorrectal. RAPD online 2009. V 32.
- Saberzadeh-Ardestani B, Foster NR, Lee HE, et al. Association of Tumor-infiltrating Lymphocytes (TILs) with Survival Depends on Primary Tumor Sidedness in Stage III Colon Cancers (NCCTG N0147) [Alliance]. Annals of Oncology; Published online 10 August 2022.
Imágenes
Adenocarcinoma Colorrectal Tipo Usual
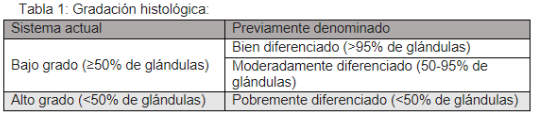
Figura 1. Adenocarcinoma colorrectal - Vista general
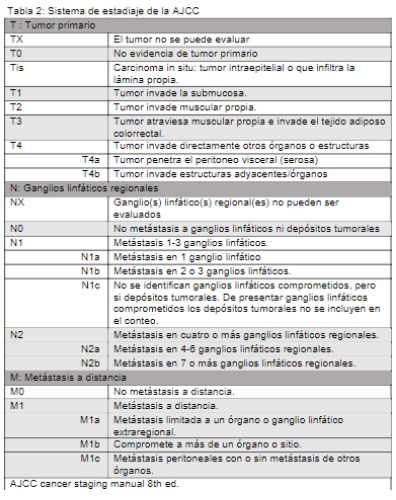
Figura 2. Detalle de atipia celular
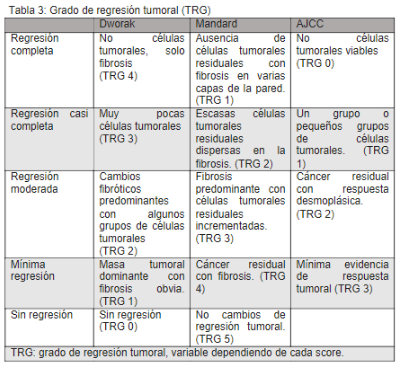
Figura 3. Estructuras glandulares irregulares
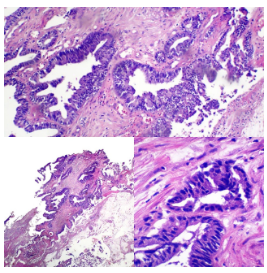
Figura 4. Necrosis sucia en lumen glandular
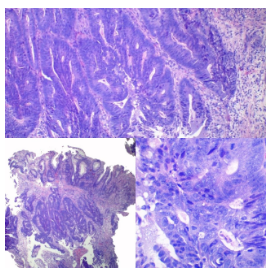
Figura 5. Crecimiento tipo "budding"
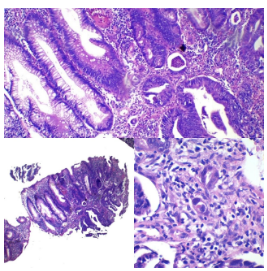
Figura 6. Desmoplasia estromal
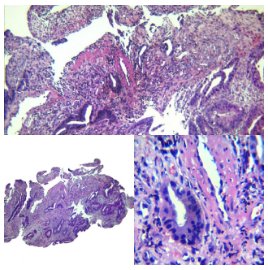
Figura 7. Linfocitos infiltrantes de tumor (TILs)
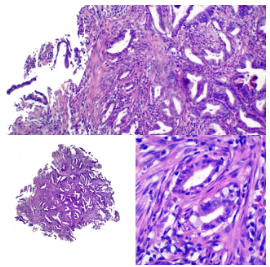
Figura 8. Carcinoma intramucoso

Figura 9. Inmunohistoquímica CK20
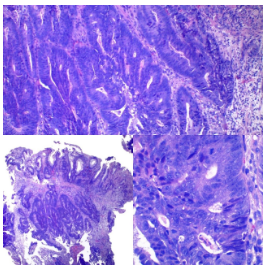
Figura 10. Inmunohistoquímica CDX2
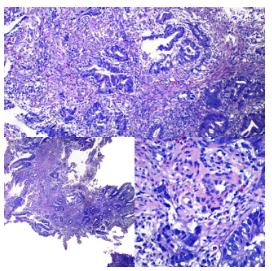
Figura 11. Inmunohistoquímica MLH1
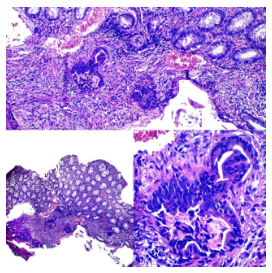
Figura 12. Inmunohistoquímica SATB2

Figura 13. Cambios post-tratamiento
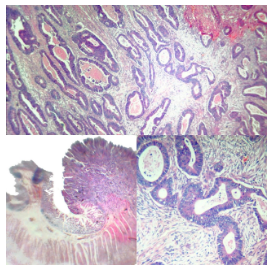
Figura 14. Regresión tumoral completa

