ADENOMA ASERRADO TRADICIONAL (TSA)
Es una lesión polipoide displásica y aserrada con riesgo de progresión a carcinoma invasivo. Su patogénesis se asocia a mutaciones en BRAF (50%) y KRAS (30%). Mientras que la progresión a carcinoma se asocia a mutaciones en CIMP (fenotipo metilador de islas CpG) o a TP53. Puede desarrollarse de novo y en un 50% de casos puede surgir de una lesión aserrada sésil o un pólipo hiperplásico (tipo células caliciformes o microvesicular). Representa el 1-2% de los pólipos colorectales y entre el 1-7% de las lesiones aserradas.
- Lesión polipoide protuberante (más frecuente)
- Lesiones planas (especialmente en colon proximal)
- Base amplia
- Superficie con textura de "piña" o patrón tipo coral
- Promedio: 10mm
- TSA avanzado: promedio 25mm (sospechar en lesiones mayores)
- Configuración exofítica con patrón velloso complejo
- Algunos casos muestran patrón plano (colon proximal)
- Aserramiento tipo hendidura ("slit-like")
- Células uniformes con citoplasma eosinofílico intenso
- Núcleos alargados (forma de lápiz), blandos, centrales
- Baja actividad mitótica
- Criptas ectópicas focales (grupos celulares similares a bases de criptas pero mal orientados)
- Células caliciformes variables (escasas excepto en subtipo rico en mucina)
- Incremento de linfocitos intraepiteliales (especialmente en TSA rico en mucina)
- Arquitectura: Glándulas apiñadas, cribiformes, necrosis intraluminal
- Población: Núcleos grandes, apiñados, hipercromáticos, pérdida de polaridad, mitosis atípicas
- Arquitectura: Glándulas pegadas con aserramiento disminuido, formación de cribas
- Población: Células eosinofílicas, cuboidales, núcleo vesicular con nucleolo prominente
- p53: Sobreexpresión (asociado a KRAS mutado)
- p16: Pérdida de expresión (asociado a BRAF mutado)
- MLH1: Pérdida en TSA avanzado con BRAF mutado
- Aserramiento tipo hendidura
- Células columnares altas con citoplasma eosinofílico intenso
- Núcleos en forma de lápiz
- TSA con displasia tipo intestinal (similar a adenoma convencional)
- TSA con displasia tipo aserrada (similar a SSL con displasia)
- TSA rico en mucina/células caliciformes: ≥50% células caliciformes
- TSA plano: Altura < 2x mucosa normal, sin proyecciones vellosas
- TSA tipo filiforme: Procesos villositarios largos con edema estromal
- TSA avanzado: Displasia intestinal de alto grado o displasia aserrada
- Alto grado
- Bajo grado
- No muestra células eosinofílicas con núcleo alargado
- No tiene aserramiento tipo hendidura
- No presenta criptas ectópicas
- SMOC1 positivo (negativo en TSA)
- Ki-67 diferente patrón
- No muestra arquitectura aserrada
- No tiene criptas ectópicas
- Pai RK, Mäkinen MJ, Rosty C. Colorectal serrated lesions and polyps. In WHO classification of Tumors Digestive system tumours. Lyon (France): International Agency for Research on Cancer, 2019. p 163-169.
- Pai RK, Bettington M, Srivastava A, Rosty C. An update on the morphology and molecular pathology of serrated colorectal polyps and associated carcinomas. Mod Pathol. 2019 Oct;32(10):1390-1415.
- McCarthy AJ, Serra S, Chetty R. Traditional serrated adenoma: an overview of pathology and emphasis on molecular pathogenesis. BMJ Open Gastroenterology 2019;6:e000317.
- Bettington ML, et al. A clinicopathological and molecular analysis of 200 traditional serrated adenomas. Mod Pathol. 2015 Mar;28(3):414-27.
- Torlakovic EE, et al. Sessile serrated adenoma (SSA) vs. traditional serrated adenoma (TSA). Am J Surg Pathol. 2008 Jan;32(1):21-9.
Imágenes
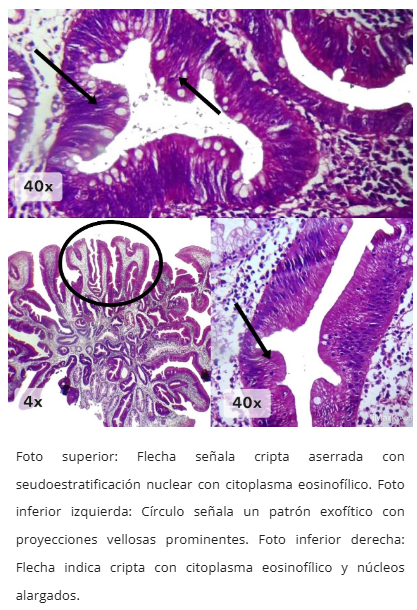
Figura 1. Adenoma aserrado tradicional - Vista general
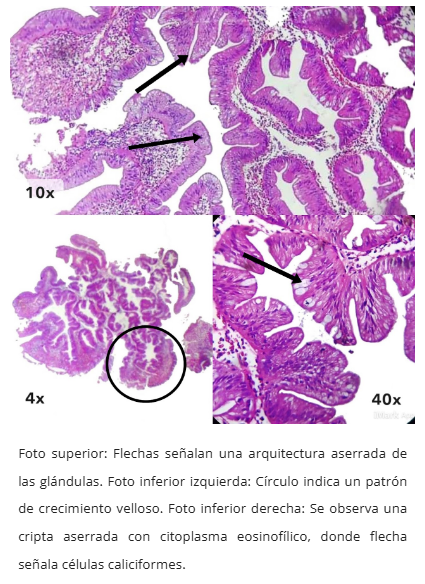
Figura 2. Detalle del aserramiento tipo hendidura
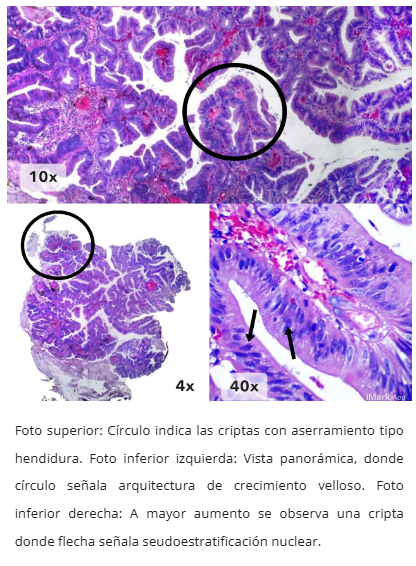
Figura 3. Células eosinofílicas con núcleos alargados
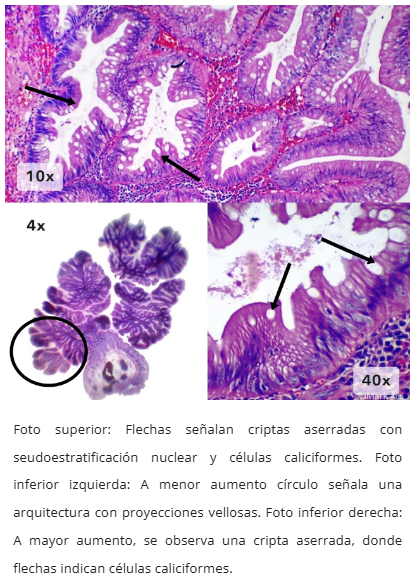
Figura 4. Criptas ectópicas características
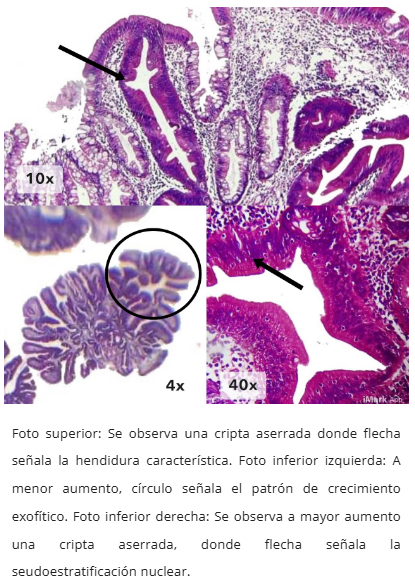
Figura 5. TSA rico en mucina/células caliciformes
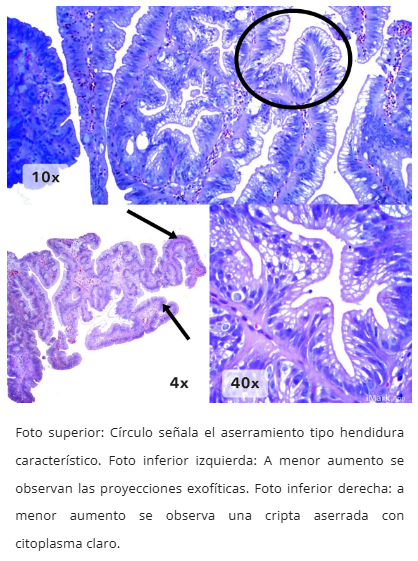
Figura 6. TSA plano (patrón de crecimiento)
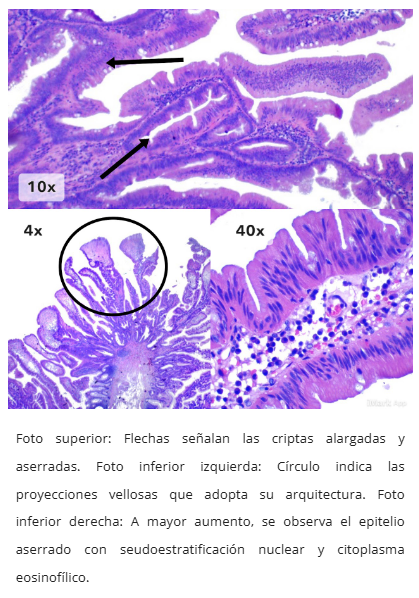
Figura 7. TSA con displasia tipo intestinal
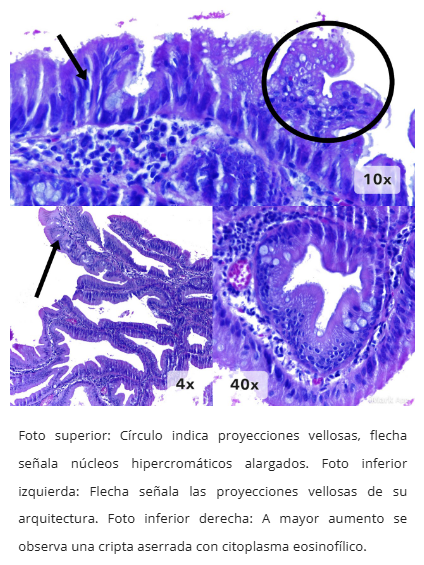
Figura 8. TSA con displasia tipo aserrada

