CARCINOMA CON ESTROMA LINFOIDE (TIPO MEDULAR)
Es una patología epitelial neoplásica invasiva en el estómago asociada principalmente a infección por Epstein-Barr virus (EBV) o a inestabilidad de microsatélite. Representa entre el 1-4% de los carcinomas gástricos. Suele tener mejor pronóstico y menor afección de ganglios linfáticos que otros subtipos, probablemente debido al gran infiltrado linfocítico del tumor. También llamado "carcinoma tipo linfoepitelioma".
1.
Endoscopía:
1.1
Localización: principalmente se localizan a nivel proximal del estómago (cardias, fondo/cuerpo).
1.2
Aspecto:
1.2.1
Lesiones tempranas: suelen presentarse deprimidas (tipo macroscópico 0-IIc) o elevadas (tipos 0-I o 0-IIa). Pueden ser múltiples.
1.2.2
Lesiones avanzadas: suelen ser ulceradas (tipo macroscópico II) o ulcero-infiltrativas (tipo III).
2.
Microscopía:
2.1
Arquitectura:
2.1.1
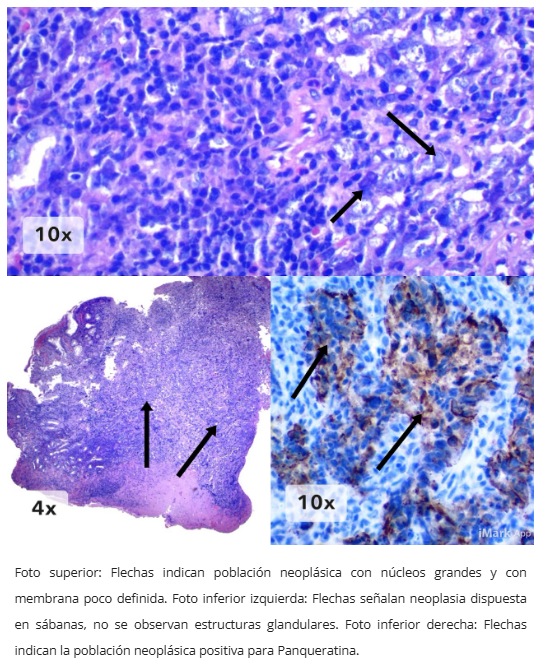
Sábanas irregulares, nidos o túbulos pobremente definidos, trabéculas o agregados sincitiales de crecimiento expansivo y bien circunscrito.
2.1.2
En estadios tempranos pueden mostrar estructuras glandulares anastomosantes o ramificadas.
2.2
Población neoplásica: alta densidad de células neoplásicas de aspecto poligonal con membranas pobremente definidas, con núcleos grandes de cromatina abierta y 1 o varios nucleolos.
2.3
Estroma:
2.3.1
Usualmente con desmoplasia mínima.
2.3.2
Marcada infiltración tumoral y peritumoral de linfocitos (mayoría CD8+).
2.3.3
Otros componentes: macrófagos, linfocitos B y células plasmáticas.
3.
Estudios complementarios:
3.1
PDL1: proteína que ayuda a las células tumorales a evitar la respuesta inmune. Tinción de membrana. Suele ser positivo, más prominente en periferia tumoral.
3.2
LMP1: proteína viral de EBV. Tinción de membrana o citoplásmica. Suele ser negativo.
3.3
MLH1, MSH2, MSH6, PMS2: proteínas reparadoras. Pérdidas combinadas sugieren inestabilidad microsatélite.
3.4
HER2: receptor de superficie. Negativo en este tipo.
3.5
CD3: proteína de membrana en células T. Positivo en linfocitos acompañantes.
3.6
CD8: marca células T citotóxicas. Linfocitos son predominantemente CD8+.
3.7
EBER (Hibridación in situ para EBV): señal nuclear fuerte en células tumorales.
4.
Criterios para el diagnóstico histológico:
4.1
Presencia de sincitios tumorales con características citológicas descritas.
4.2
Estroma con extensa infiltración linfocítica.
5.
Gradación histológica: No se ha identificado un sistema de gradación específico.
6.
Tipificación:
6.1
Asociado a inestabilidad de microsatélite
6.2
Asociado a Epstein Barr virus
6.3
Sin positividad para EBV ni inestabilidad de microsatélites (mayor diferenciación glandular)
7.
Estadiaje: se realiza según sistema AJCC descrito en apartado de adenocarcinoma gástrico.
8.
Referencias:
- Hissong E, Ramrattan G, Zhang P, et al. Gastric Carcinomas With Lymphoid Stroma: An Evaluation of the Histopathologic and Molecular Features. Am J Surg Pathol. 2018;42(4):453-462.
- WHO classification of Tumors Digestive system tumours. Lyon (France): International Agency for Research on Cancer, 2019.
- Park YS, Kook MC, Kim Bh, et al. A standardized pathology report for gastric cancer: 2nd edition. J Pathol Transl Med. 2023;57(1):1-27.
- Shin DH, Kim GH, Lee BE, et al. Clinicopathologic features of early gastric carcinoma with lymphoid stroma and feasibility of endoscopic submucosal dissection. Surg Endosc. 2017;31:4156-4164.
- Huh CW, Jung DH, Kim H, et al. Clinicopathologic features of gastric carcinoma with lymphoid stroma in early gastric cancer. J Surg Oncol. 2016;114(6):769-772.
- Iwasaki K, Suda T, Takano Y, et al. Postoperative outcomes of gastric carcinoma with lymphoid stroma. World J Surg Onc. 2020;18:102.
Imágenes
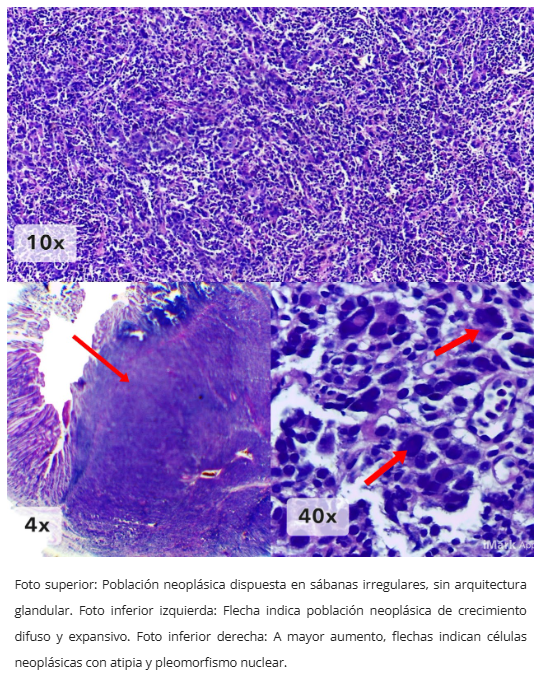
Carcinoma medular - Visión general
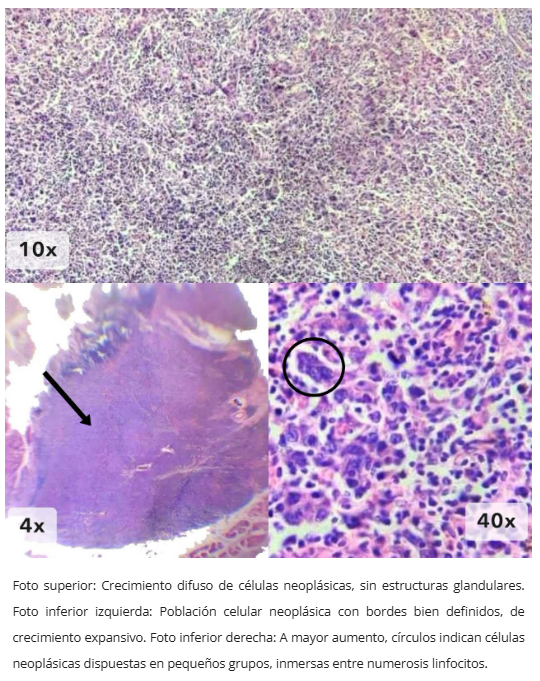
Marcado infiltrado linfocítico
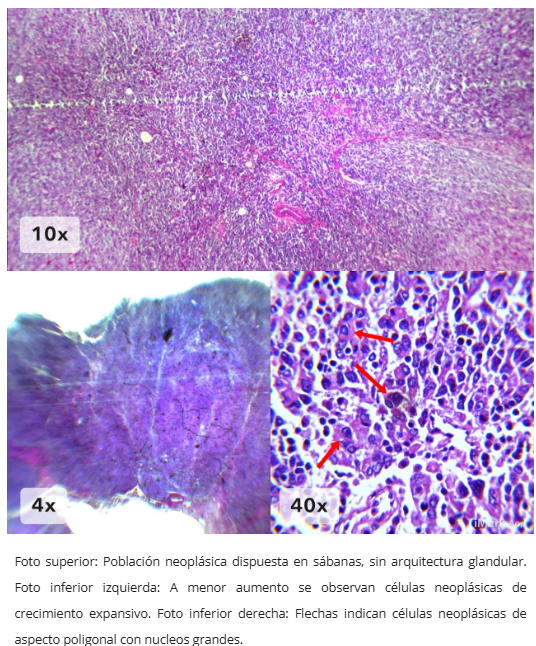
Células neoplásicas poligonales
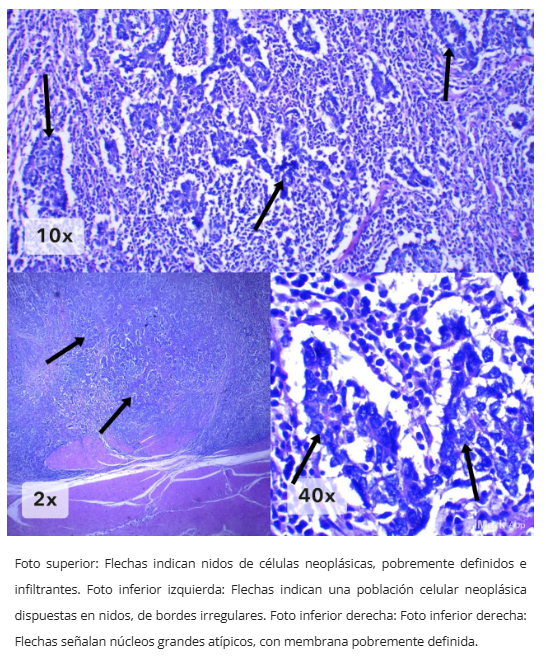
Hibridación in situ EBER (EBV)
Inmunotinción CD8 (linfocitos citotóxicos)






