TUMOR DEL ESTROMA GASTROINTESTINAL (GIST)
Es una patología neoplásica mesenquimal de comportamiento incierto. Se originan a partir de células intersticiales de Cajal o de un subconjunto similar de células madre. Su patogénesis se asocia a mutaciones en los genes KIT o PDGFR (>85% casos). La mayoría surgen de mutación esporádica, mientras que un 5% se asocia a síndromes como la Triada de Carney o el síndrome de Carney-Stratakis.
-
1.
Endoscopía:
-
1.1
Localización: Puede ocurrir a cualquier nivel del TGI desde la mitad distal del esófago hasta el área ano-rectal. Más de la mitad se localizan en estómago (cuerpo y fondo más que antro).
-
1.2
Aspecto:
- Lesiones firmes, fijas o móviles
- Tamaño variable (desde milímetros hasta >20cm, promedio 6cm)
- Usualmente únicos (pueden ser múltiples en casos especiales)
- En ecoendoscopía: lesiones sólidas hipoecóicas, bien delimitadas
- Patrones de crecimiento: intraluminal, extraluminal o mixto "reloj de arena"
-
1.1
-
2.
Microscopía:
-
2.1
Arquitectura: Nodular no encapsulado, bien delimitado, submucoso o en capa muscular. Patrones:
- Organoide o en nidos
- Fascicular o arremolinado (tipo fusocelular)
- Pseudopapilar (tipo epitelioide)
-
2.2
Población tumoral:
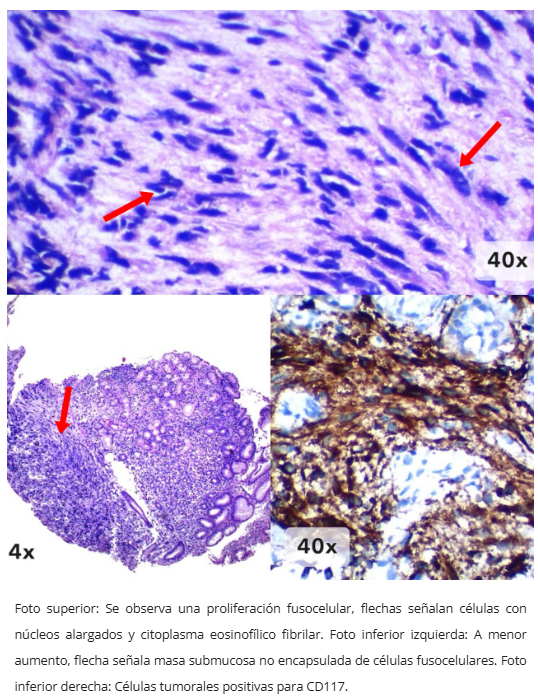
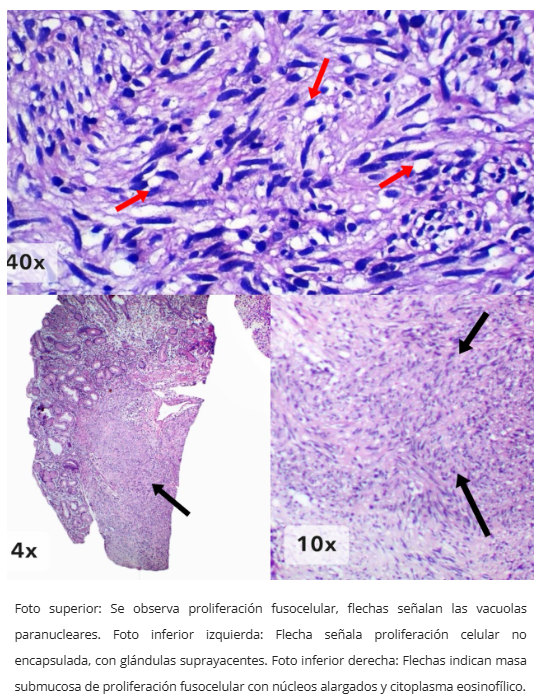
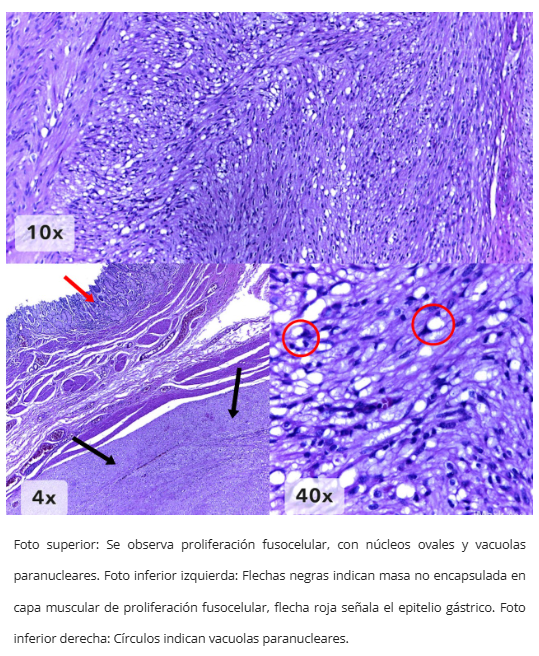
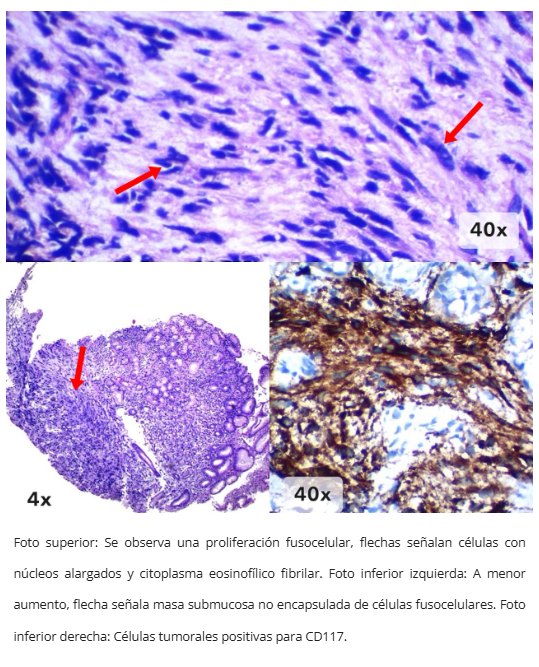
- Fusocelular (más frecuente en estómago): citoplasma eosinofílico fibrilar con vacuolización paranuclear
- Epitelioide (más en antro): citoplasma eosinofílico a claro, núcleo redondo
- Mixto: transición abrupta entre ambos componentes
-
2.3
Estroma: Puede mostrar cambios escleróticos, mixoides, colagenosos o degeneración quística. Fibras skenoides (más frecuentes en intestinal).
-
2.1
-
3.
Inmunohistoquímica:
- CD117/KIT: Positividad citoplásmica intensa (95% gástricos, 98% intestinal)
- DOG1: Útil para casos KIT negativos (positivo en 50% de estos)
- PDGFRA: Positivo en GIST con mutación PDGFRA
- CD34: Positivo en 85-90% GIST gástricos fusocelulares
- Marcadores musculares: Actina positiva en 20% (gástricos), desmina raramente positiva
- Marcadores neurales: S100 positivo en 14% intestinal, <1% gástrico
-
4.
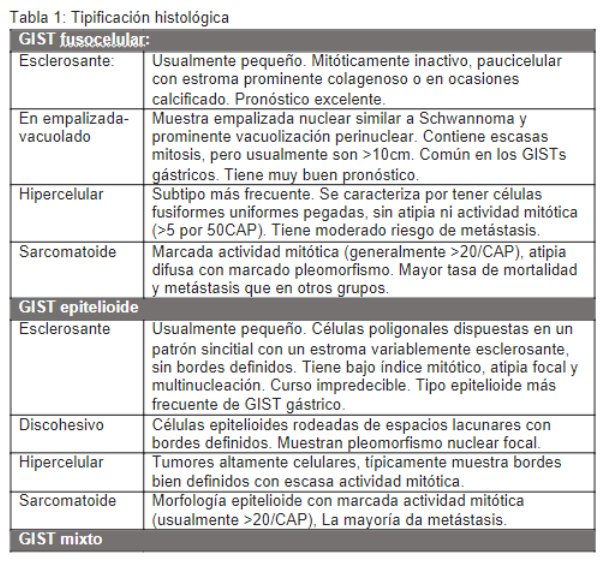
Criterios diagnósticos (WHO 2019):
- Masa intramural, submucosa o subserosa
- Morfología fusocelular, epitelioide o mixta
- Inmunopositividad para KIT y/o DOG1
- Pérdida de SDHB en GISTs SDH deficiente
-
5.
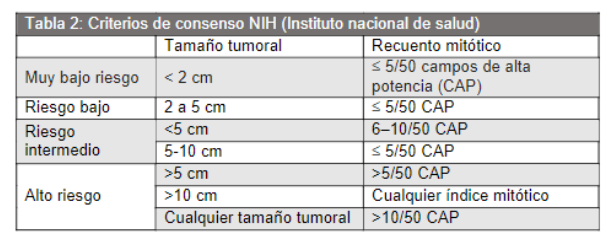
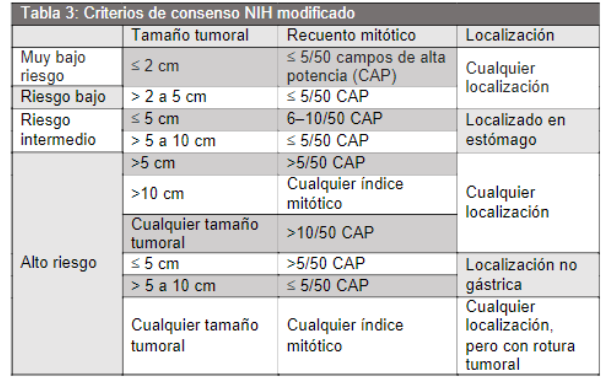
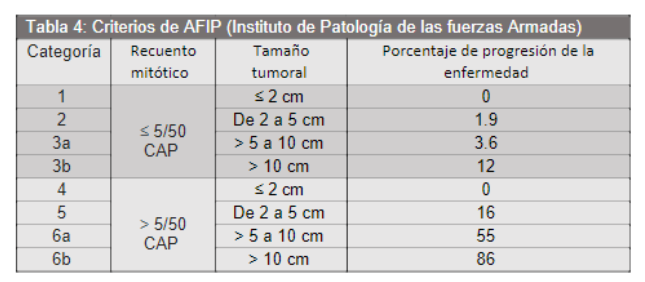
Gradación y pronóstico: Factores principales:
- Tamaño tumoral (>2cm mayor riesgo)
- Conteo mitótico
- Localización (gástrico mejor pronóstico)
-
6.
Diagnóstico diferencial:
-
6.1
Leiomiomas/leiomiosarcomas: Positivos a desmina, usualmente negativos a CD117
-
6.2
Fibromatosis desmoide: Positiva para beta catenina, mutaciones APC
-
6.3
Tumor miofibroblástico inflamatorio: Positivo a ALK-1, negativo CD117
-
6.4
Schwannomas: Positivos a S100, GFAP, negativos a CD117
-
6.1
-
7.
Referencias:
- 7.1 Dei Tos AP, et al. WHO Classification of Tumors Digestive system tumours. 2019.
- 7.2 Foo WC, et al. Pathology of gastrointestinal stromal tumors. Clin Med Insights Pathol. 2012.
- 7.3 Martin-Broto J, et al. SEAP-SEOM consensus on pathologic and molecular diagnosis. Clin Transl Oncol. 2017.
- 7.4 Miettinen M, Lasota J. Gastrointestinal stromal tumors. Gastroenterol Clin North Am. 2013.
- 7.5 Parab TM, et al. Gastrointestinal stromal tumors: a comprehensive review. J Gastrointest Oncol. 2019.
- 7.1
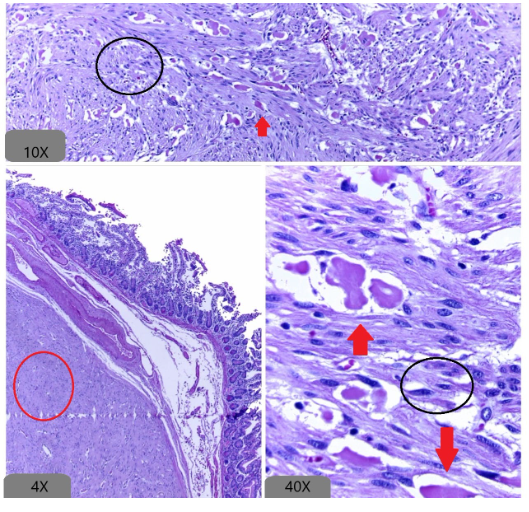
Imágenes de Referencia
GIST fusocelular con vacuolización paranuclear
GIST epitelioide con patrón pseudopapilar
GIST mixto (fusocelular y epitelioide)
Tinción positiva para CD117 (KIT)
Tinción positiva para DOG1
Patrón de crecimiento "reloj de arena"
GIST SDH deficiente
Fibras skenoides (PAS positivo)
GIST metastásico en hígado

